
受験生の皆さん、こんにちは。
東大合格ビジネスマンのワタシですm(_ _)m
私のブログでは
① 入試問題の解答・解説
② 受験合格に必要なマインド
③ 3大基礎力重視の裏ワザ勉強法
について、様々な情報を発信しております📢
私の公式LINEでは、無料相談を随時受け付けております。
公立中出身から東大理Ⅲ,京大医学部のA判定に辿り着いた私が、大手予備校や受験秀才が言わない情報を存分に発信します。
成績が低迷しているのに1人で悩むのは時間の無駄ですから、受験のプロを頼ってください✊
私も苦手科目は先生に頼りました。
また、LINE登録していただいた方には
無料プレゼント(1年で偏差値70出す画期的勉強法)
を贈呈します🎁
【⬇️公式LINE登録はこちら⬇️】

2021年入試、旧帝大の第6弾は
「京都大学」です。
当ブログの解説記事は
読者が必死に3年間努力すれば
東大(理三以外)・京大(医以外)・九大医
レベルに80%以上の確率で合格できる
ことを目的に作成しています
市販の問題集のように、解法を丁寧に示すだけではありません!多角的なアプローチで問題を解きほぐしています✊
① 各問の難易度
② 他分野や一般常識との関連事項
③ 問題の躓きポイント
④ 極力曖昧な表現をしない説明
を示しています。
イマイチ成績が突き抜けられない受験生に貴重な情報が提供できればと思いますm(__)m
京大化学の特徴
京都大学の理科は2科目で180分。そのうち、物理は全3問です。理科180分て長くない??
いやいや👋
下手に学力あって全問解きにいくと
情報処理に、計算処理に
思い切り時間食われて
むしろ足りない
です🚩
今年の化学には、物議を醸した凶悪な大問が存在します。さて、それは第1~4問のどれでしょう😅❓
学習を積んできた人なら簡単にわかりますよ。
そして、先に謝罪しておきますが、凶悪な大問については私自身解けず終いのため、解答は途中で終わっておりますm(__)m
内容をきちんと消化するには
全統記述模試の偏差値63~68程度
の実力が欲しいですね。
第1問



【解答】
(問1) 易~やや易
(ア) Cu²⁺、(イ) 還元、(ウ) I⁻
(エ) 酸化、(オ) I₂、(カ) I₃⁻
<分析>
水溶液中にはCu²⁺,I⁻が存在します。CuI(Cuの酸化数+1)が生じたので、「Cu²⁺は還元され、I⁻は酸化される」と解釈できます🤔
さらに、I₂とI⁻が共存するとき、I₂+I⁻⇔I₃⁻の反応により水溶液は褐色となります☝
(問2) 標準
2Cu²⁺+5I⁻ → 2CuI+I₃⁻
<分析>
「I₂+I⁻⇔I₃⁻の平衡は完全に右に偏る」から意識すべきことは?そこを解釈できたかがポイントでした💡
本来なら右辺にI₂がくるのでしょうけど、I₂は残りのI⁻と反応してI₃⁻を生じると解釈しないといけないので、右辺にはI₃⁻がきます☝
(問3) 標準
I₃⁻+2S₂O₃²⁻→S₄O₆²⁻+3I⁻
<分析>
(酸化剤) I₂+2e⁻→2I⁻・・①
(還元剤) 2S₂O₃²⁻→S₄O₆²⁻+2e⁻・・②
①+②より
I₂+ 2S₂O₃²⁻→S₄O₆²⁻+2I⁻
ここで、平衡は完全に右に偏るため、I₂でなくI₃⁻を表記するので、両辺にI⁻を足すと、答になります。
(問4) やや易
9.10 (mol)
<分析>
S₂O₃²⁻と反応したI₂は、0.1×18.2×10⁻³×1/2=0.91×10⁻³(mol)。[実験1]でCu²⁺1(mol)からI₂が0.5(mol)生じるので、電気分解後のCuSO₄水溶液2ml中にあったCu²⁺は0.91×10⁻³×2=1.82×10⁻³(mol)。
∴ 溶液10L中のCu²⁺は
1.82×10⁻³×10⁴×1/2 =9.10(mol)。
S₂O₃²⁻と反応したI₂は、0.1×18.2×10⁻³×1/2=0.91×10⁻³(mol)。[実験1]でCu²⁺1(mol)からI₂が0.5(mol)生じるので、電気分解後のCuSO₄水溶液2ml中にあったCu²⁺は0.91×10⁻³×2=1.82×10⁻³(mol)。
∴ 溶液10L中のCu²⁺は
1.82×10⁻³×10⁴×1/2 =9.10(mol)。
(問5) やや易
-log₁₀Ka
<分析>
緩衝作用が最大なのは[CH₃COOH]=[CH₃COO⁻]のとき。これは経験的にわかるはずです(笑)また、Ka=[CH₃COO⁻][H⁺] / [CH₃COOH]より、[H⁺]=Ka。
∴pH=-log₁₀[H⁺]=-log₁₀Ka
pHの定義式は覚えましょう💡
(問6)
(a) 2H₂O→O₂+4H⁺+4e⁻
(b) Cu²⁺+2e⁻→Cu
<分析>
陽極では水の電気分解、陰極ではCu²⁺の還元が行われます👇
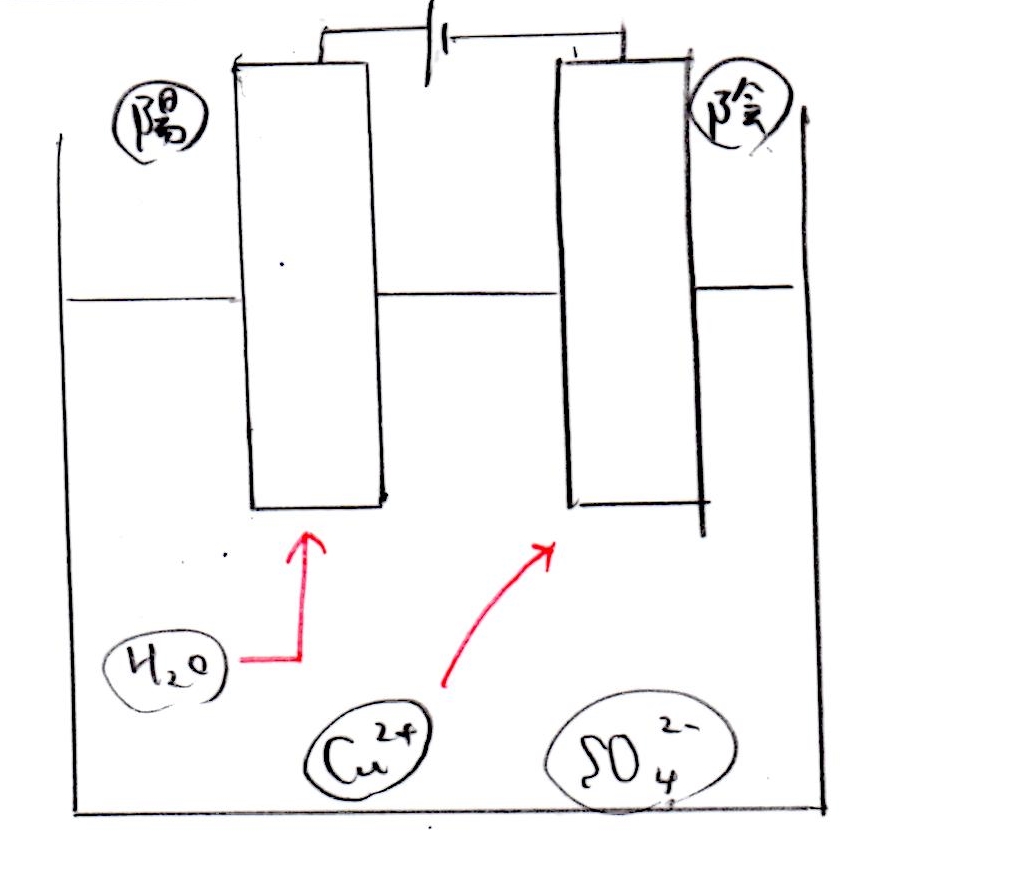
(問7)
1.00 (mol)
<分析>
流れた電子は193×10³/9.65×10⁴ =2.0(mol)なので、析出するCuの理論量は、2×1/2 =1.00(mol)。
(問8)
90(%)
<分析>
実際に利用されたCu²⁺は1.0×10-9.10=0.90(mol)。
∴求める効率は100×0.9/1.0=90%。
<感想>
今年の第1問はめっちゃ普通の酸化・還元と電気分解の問題でした⚡
ただ、1つtrapが存在してましたね。「I₂+I⁻⇔I₃⁻の平衡は完全に右に偏る」のところ。ここの表現意図を汲み取れなかった方、結構いるのでは?
とにかく、後に控える第2問が凶悪なのもあり、ここは高得点を収めたいところですね👊
第2問
解答は問1,問2,ルシャトリエ(笑)だけです💦

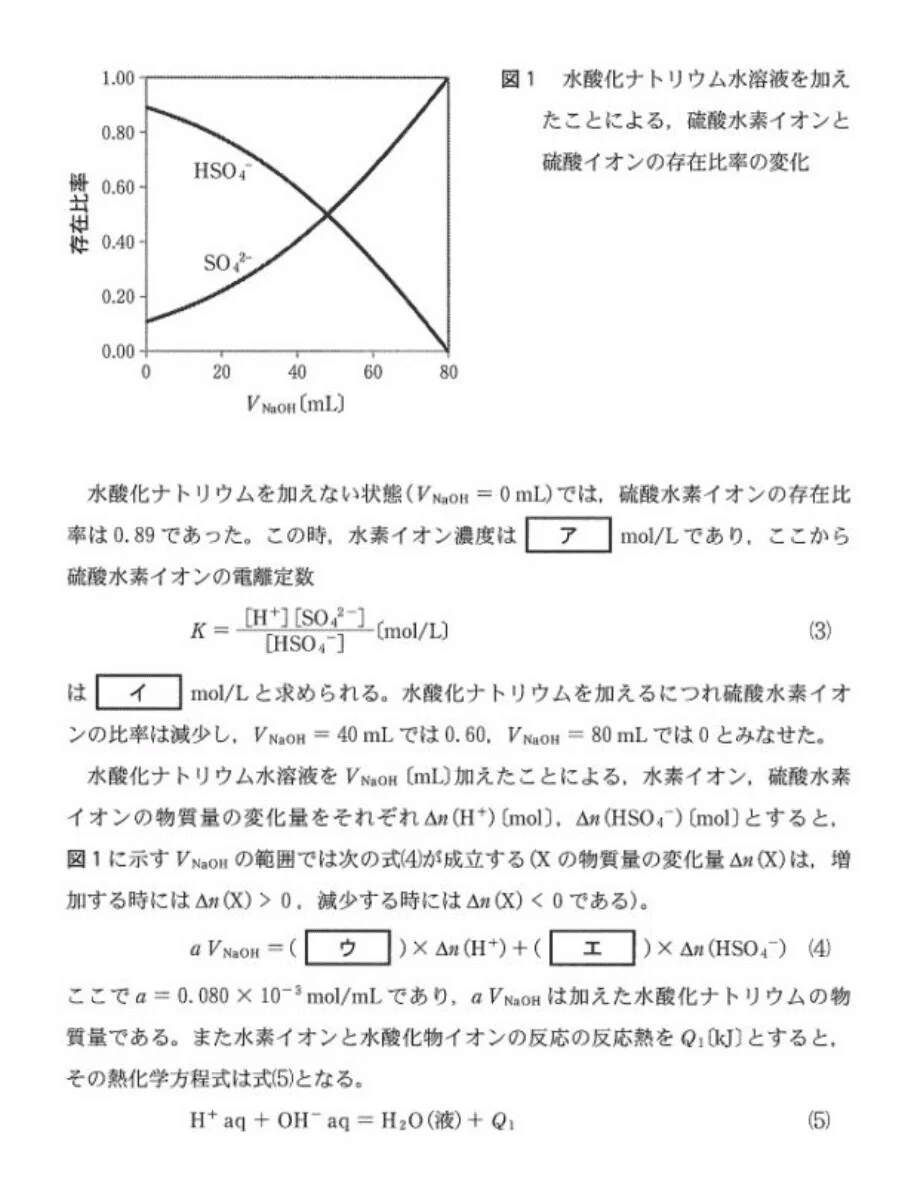

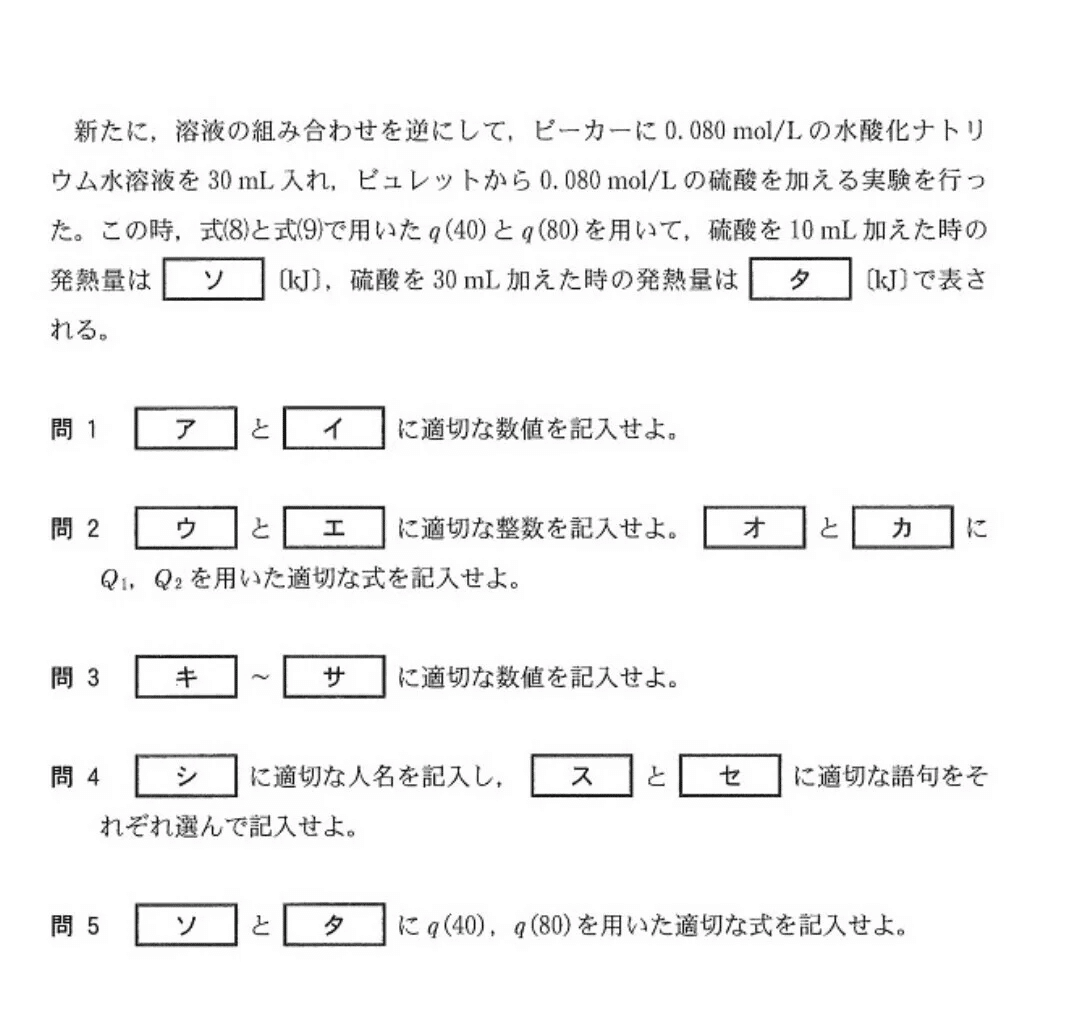
【解答】
(問1) やや易〜標準

<分析>
第1電離が完全に起きた状態から、第2電離がどれくらい起きたのかを調べにいきます✊
すると、電離で生じたH+のモル濃度がわかり、平衡定数Kもわかります。
(問2) やや難

<分析>
どう考えてよいか非常にわかりづらいです。
1つの考え方としては、解答のように展開できるでしょう。ただ、それ以降はわからず😵
(問4-シ) 易
ルシャトリエ
<感想>
物議を醸した凶悪の第2問です。
正直、問1と問4(シ)を取って、(ス)(セ)は2択だから運で片方合わせればOKでしょう。それ以外は医学部でさえ落として問題ないです(笑)
私もマジでわかりませんでした(;’∀’)
なので、解説も途中で終わってます💦
第3問


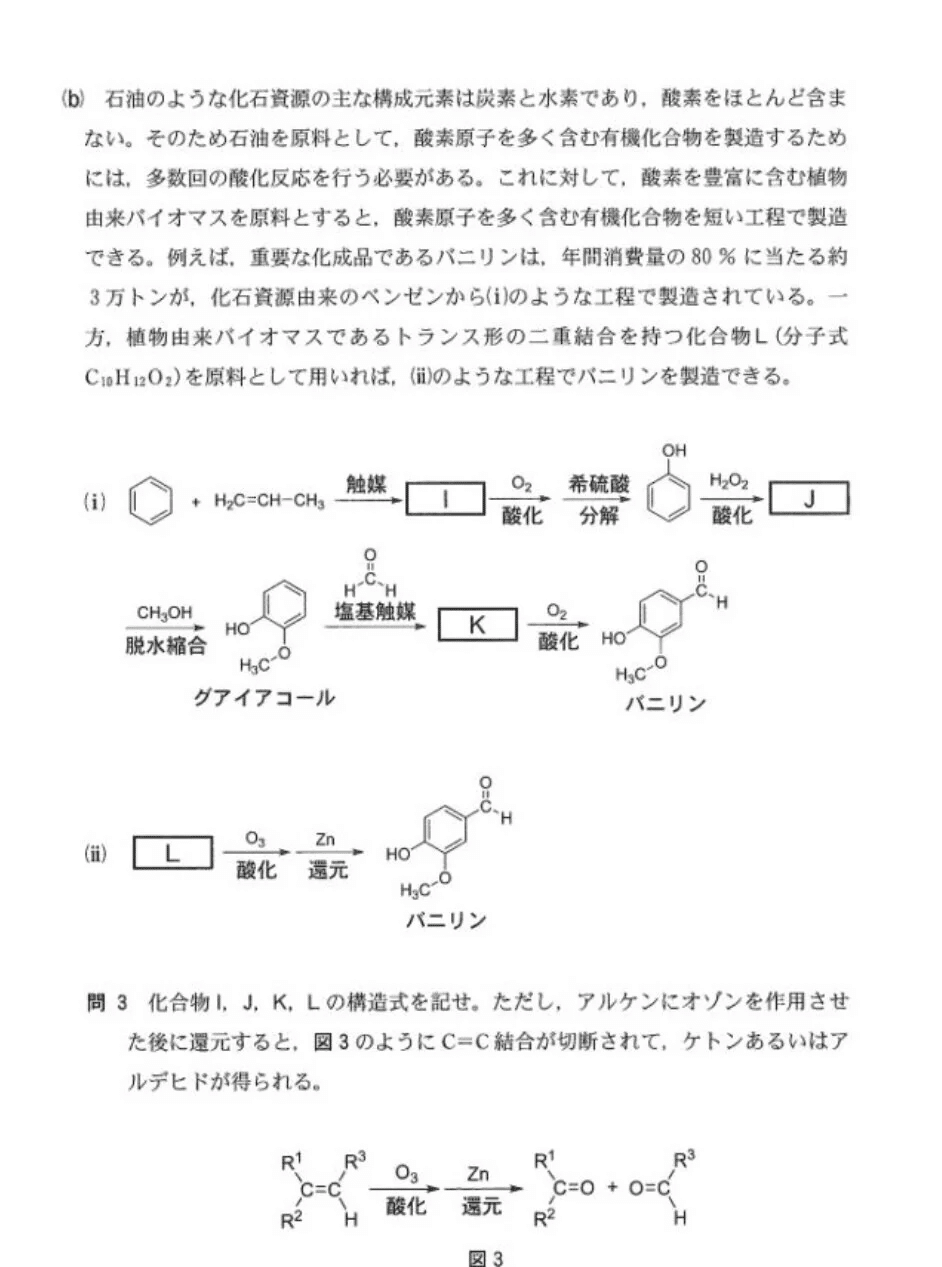
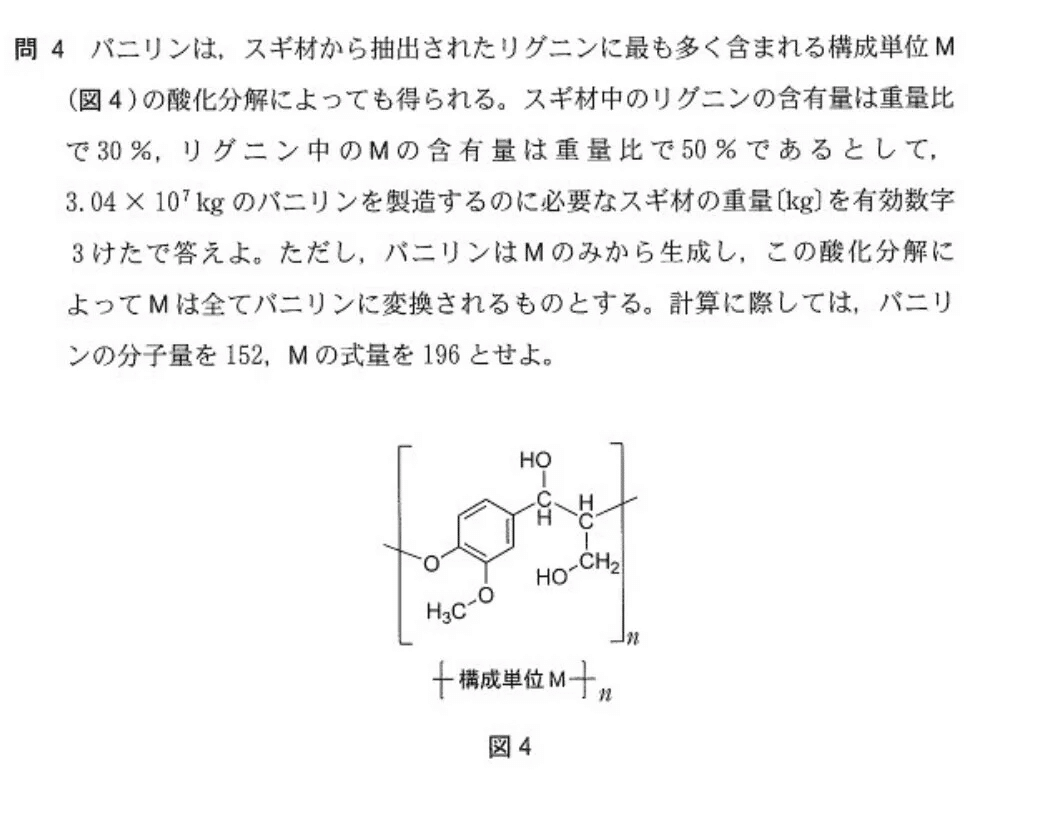
【解答】
(a)
《情報整理》

(問1) 標準
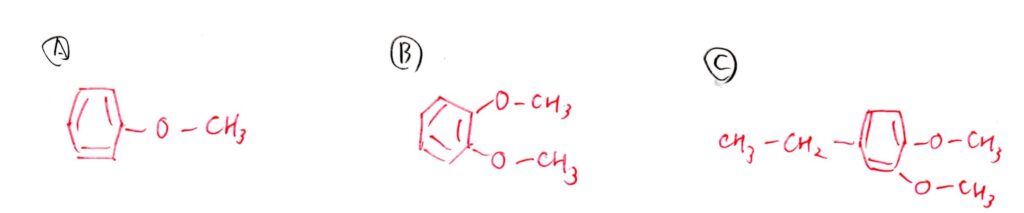
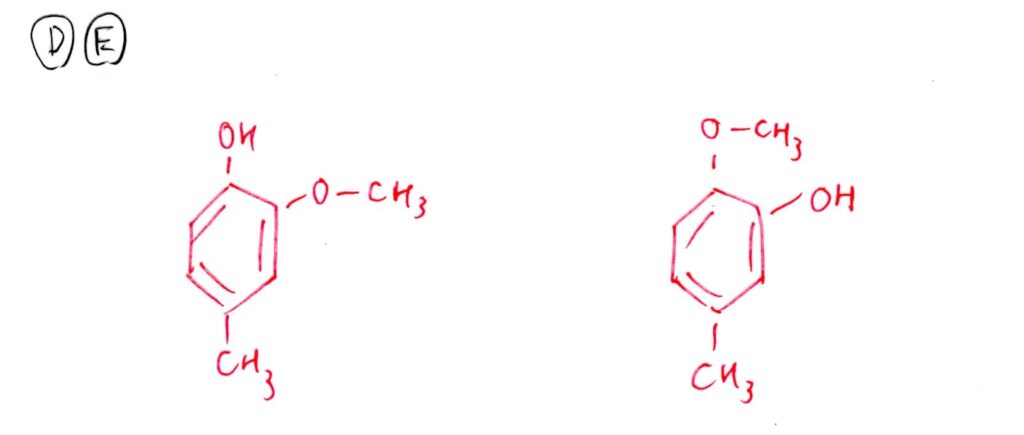
<分析>
A,Bは縮合させる物質が明示されているため簡単。Cがやや手強いです💧
「過マンガン酸カリウムで酸化→炭化水素基を-COOHに変える」
「熱分解でCO₂が脱離→-COOHが-Hに変わる」
この2点を認識できたかが、合否の分かれ目だったかも🤔
D,Eについては、炭素数8とFの構造式をもとに導出できると思います。
(問2) 標準
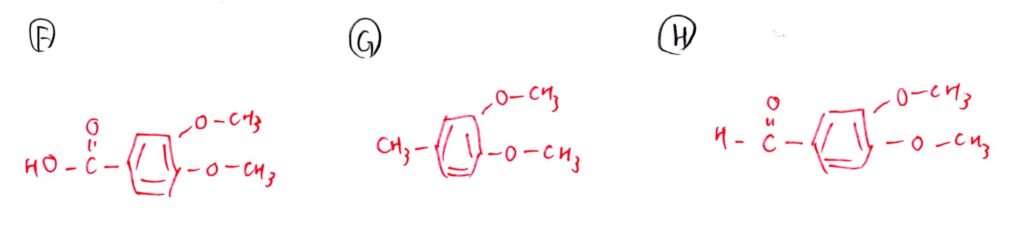
<分析>
F,G,Hは(問1)を解く過程で出てくるので、実質(問1)ができれば芋づる式に解けます☝
(b)
《情報整理》
(問3)

<分析>
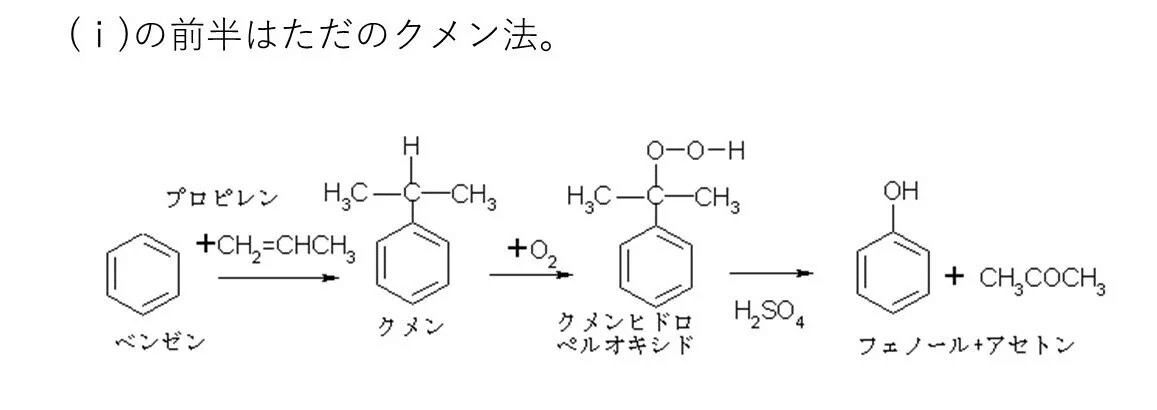
Iはクメン法そのもの。知っていれば簡単!
Jは一瞬「何これ?」と思ったでしょうけど、置換基が2個に増えている点から-OHが2つになったのでは?と推測したいところです🤔
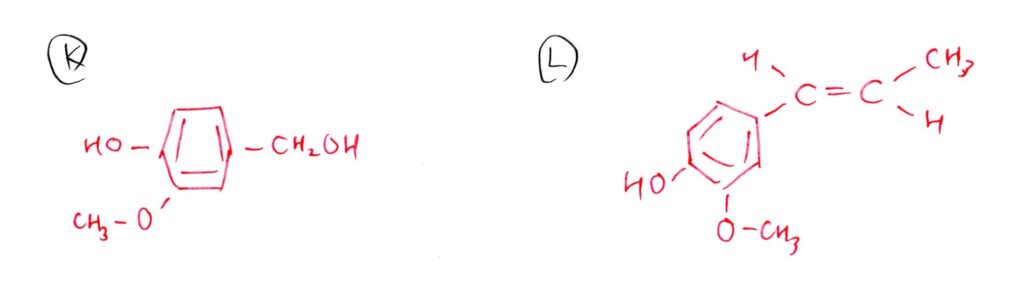
Kは「フェノール樹脂で似たような反応あったなぁ・・」と思えれば勝ち。既存知識は大事。
Lはオゾン分解を理解していれば、炭素数10より、構造は1に決まります!
(問4) やや易
2.61×10⁸(kg)

<分析>
Mの構成単位は与えられており、分子量は簡単にわかります。よって、ただの計算問題。
<感想>
(問1)は情報整理が厄介なら図示化と箇条書きを勧めます。
内容自体はめっちゃ標準的で特に言うことないけど、「京大に受かるか落ちるかの試金石が問1かなぁ~」て思います。
第4問





【解答】
(a)
(問1) 易~やや易
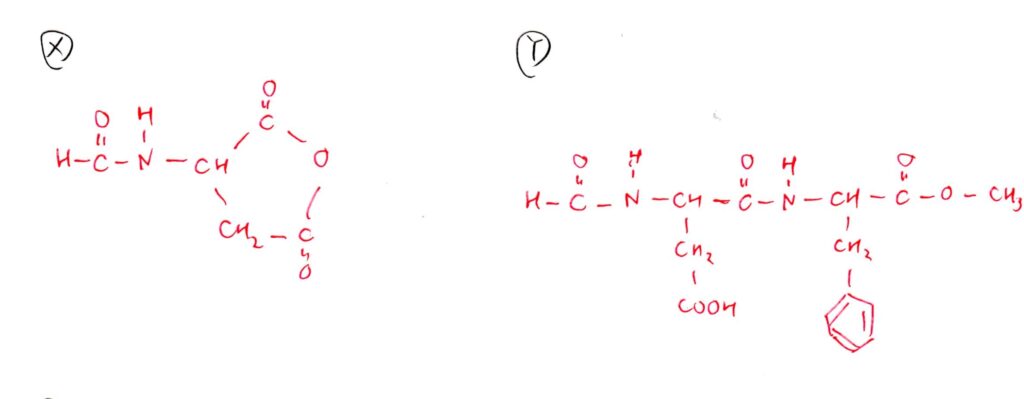

<分析>
合成法の通りに作業するだけの簡単な問題です(笑)
(問2) 易~やや易

<分析>
Yのギ酸を離脱させたものです。
(問3) 標準~やや難
グルタミン酸、プロリン
<分析>
②より、pH=6で陰イオンになっているもの ⇒ 酸性アミノ酸の存在。でも、アスパラギン酸、グルタミン酸のどっち??もう1つのアミノ酸についても情報なし。
ここで、炭素数で考える!
ヒスチジンの炭素数は6より、残り2つの炭素数は計10。アスパラギン酸を選ぶとすると、他に炭素数6のものがなく不適!!
よって、グルタミン酸とプロリンで決まり◎
(問4) やや易
(a) カルボキシ、(b) 酸性
(c) 4、(d) 負

<分析>
ただの酸性アミノ酸の理解度チェックです☝
(問5) やや易
(ⅰ)
無水酢酸
(ⅱ)
ラクタムが加水分解されて生じるアミノ酸が、無水酢酸によりアセチル化されるから。
<分析>
アセチル化が何かわかっていれば、無水酢酸は簡単に出てくるはず。
(ⅱ)はわざわざ「ラクタム」を使えという指示があるので、解答の方向性はつかみやすいでしょう。
(問6) やや難~難
グルタミン酸-ヒスチジン-プロリン
<分析>
順番はすんなり決まってくれません💦丁寧に検討していく必要があるようです🤔
①
「ラクタム」「-NH₂がない」に着目すると・・分子内でアミド結合しうるのは、-COOHを2つもつグルタミン酸のみ。
②
一般にN末端のNH₂はアセチル化されるのに、今回はしていない。つまり、グルタミン酸がN末端にあり、かつラクタムを形成する。
③
(キ)より、ヒスチジンがC末端だとそもそも分解しない。
(問7) やや難~難

<分析>
(問6)がわかれば自動的にできる問題なんですが、その(問6)が難しいのです💦
-COOHとNH₃を反応させると、-CONH₂の形ができます☝
<感想>
問5までは易しめでそれなりに得点しやすいものの、問6,7が結構考えさせられますね😅
問6は「N末端のNH₂がラクタム形成が原因で存在しない」「それが可能なのはCOOHが2個あるグルタミン酸」である点に気付くのが難しいです💦
総括
第2問が凶悪のため80%以上の得点は困難です!!
私も発熱Qのとこから意味不明になりました(+_+)でも、問1とルシャトリエは取りましょう(笑)
全体的には、簡単めの第1問と第3問をほぼ完答して、第4問は問5まで確実に取れば、医志望でも問題ないかと思います。
ボーダーは
非医:50%
医:65%
程度でしょう。
いずれにせよ、第2問を最低限取って、他取れるところは絶対落とさない戦法が一番良かったでしょう😅
最後に、再度公式ラインの紹介をします。
私の公式LINEでは、無料相談を随時受け付けております。
成績が低迷しているのに1人で悩むのは時間の無駄ですから、受験のプロを頼ってみてください✊
【⬇️公式LINE登録はこちら⬇️】





