
受験生の皆さん、こんにちは。
東大合格ビジネスマンのワタシですm(_ _)m
私のブログでは
① 入試問題の解答・解説
② 受験合格に必要なマインド
③ 3大基礎力重視の裏ワザ勉強法
について、様々な情報を発信しております📢
2022年大学入試、旧帝大の第6弾は
「大阪大学」
です。
当ブログの解説記事は、読者の成績を最難関レベルまでグングン伸ばすことを目標にしており
読者が必死に3年間努力すれば
東大(理三以外)・京大(医以外)・九大医
レベルに80%以上の確率で合格できる
ことを目的に作成しています✊
市販の問題集のように、解法を丁寧に示すだけではありません!多角的なアプローチで問題を解きほぐしています✊
① 各問の難易度
② 他分野や一般常識との関連事項
③ 問題の躓きポイント
④ 極力曖昧な表現をしない説明
を示しています。
イマイチ成績が突き抜けられない受験生に貴重な情報が提供できればと思いますm(__)m
私の公式LINEでは無料相談を随時受け付けております。公立中出身から東大理Ⅲ,京大医学部のA判定に辿り着いた私が、大手予備校や受験秀才が言わない情報を存分に発信します。
成績が低迷しているのに1人で悩むのは時間の無駄ですから、受験のプロを頼ってください✊
私も苦手科目は先生に頼りました。
また、LINE登録していただいた方には、無料プレゼント(1年で偏差値70出す画期的勉強法)を贈呈します🎁
無料相談もどしどし受け付けております✊
【⬇️公式LINE登録はこちら⬇️】

阪大化学の特徴
大阪大学の理科は2科目で150分。一問一答型の問題がほとんどですが、問題把握や計算処理に時間を要し、時間的余裕はありません✋
そのうち化学は全4問で、第1,2問は理論化学(無機)、第3問は有機化学、第4問は高分子化合物です。3問だと物理より楽なんですが、4問だと物理よりも時間的に重いんですよね😅

なお、第3問は分子式の可能性が複数あり、問1で躓くと後が崩壊する内容だったので、本記事では削除とさせていただきましたm(__)m
詳しくはコチラ参照👇
第1問



【解答】
(問1) 易~やや易
(1)

(2)
(ア) カルシウム
(イ) Ca(HCO₃)₂
(ウ) CaCO₃
<分析>
(2)は鍾乳洞形成の過程を表しています。難関大学では記述問題で出題されたりするので、よ~く理解を深めておきましょう💡
(鍾乳洞のでき方)
(山口県 秋芳洞)

(問2)
(1) 易
2NO+O₂ → 2NO₂
<分析>
COが酸化されてCO₂になる反応式と同じように書けばOKです。
また、Nの酸化数変化に着目してNO→NO₂の反応を考えてもいいですね。
(2) やや易
Cu+4HNO₃ → Cu(NO₃)₂+2H₂O+2NO₂
<分析>
本問の要点は「希硝酸でNO,濃硝酸でNO₂」です。それがわかれば後は係数比較で出せます。
もちろん係数も含めて覚えておいた方が速いのですが💦
(3) 標準

<分析>
まず、分子がN₂O₄であることを予測できないと厳しいと思います。
でも、演習量を積んでいれば2NO₂⇔N₂O₄の平衡反応はもはや常識でしょう。
ちなみに、下記のNO₂を2つ結合させてもN原子の周りには6個の電子しかありません。
これを上手く操作してN原子の周りの電子を8個にしようとすると・・・N-O結合の1とをN=O結合に変化させてやるとよいですね。

(4) やや易
(エ) 共有
(オ) 非共有
(カ) NO₂⁺
(キ) NO₂
(ク) NO₂⁻
<分析>
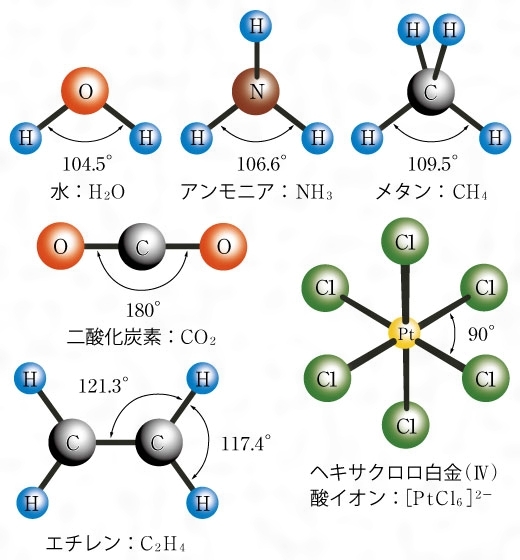
結合角がCH₄>NH₃>H₂Oとなる話題も難関大受験生にとっては有名な話でしょう。
不対電子-共有電子対の反発力は、非共有電子対と共有電子対の反発力より弱いことを問題文から読み取れば、(カ)~(ク)は決まります。
(結合角)
(問3) 易~やや易
(ケ) イオン化
(コ) 自由
(サ) 金属
(シ) 14
(ス) 4
(セ) 5
(ソ) 1
<分析>
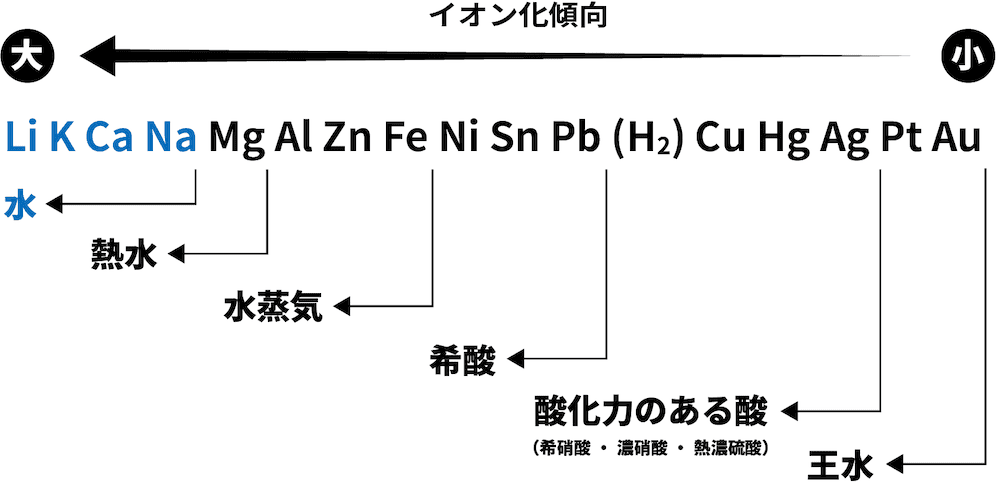
(ケ)以外は楽勝でしょう。(ケ)は「金属イオンは陽性が強い」から、「陽イオンになりやすい ⇒ イオン化エネルギーが小さい」と判断したいですね🚩
(問4)
(1) 易~やや易

<分析>
テルミット反応、Al₂O₃,Fe₂O₃の生成反応は余裕で書けるでしょうし、ただの引き算なので、全然楽勝でしょう!
(2) やや易

<分析>
「陰極の反応式を書く⇒電子の物質量を求める⇒電気量に換算する」のお馴染みの解法でした。
(3) やや易
Alの方がFeよりもイオン化傾向が大きく、さらに(1)の反応が発熱反応であるから。
<分析>
イオン化傾向の説明だけでもよさそうなのですが、地味に字数が足りないので、(1)の結果も解答に反映させました。
<感想>
(問1)~(問4)まで幅広く典型問題をかき集めました~という感じが否めません(笑)
頭を捻るとすれば、(問2)(3)くらいでは?他は、基礎理解が徹底されていれば、全然間違う要素のない問題であり、得点源にしておきたい大問ですね。
第2問


【解答】
(問1) やや難〜難
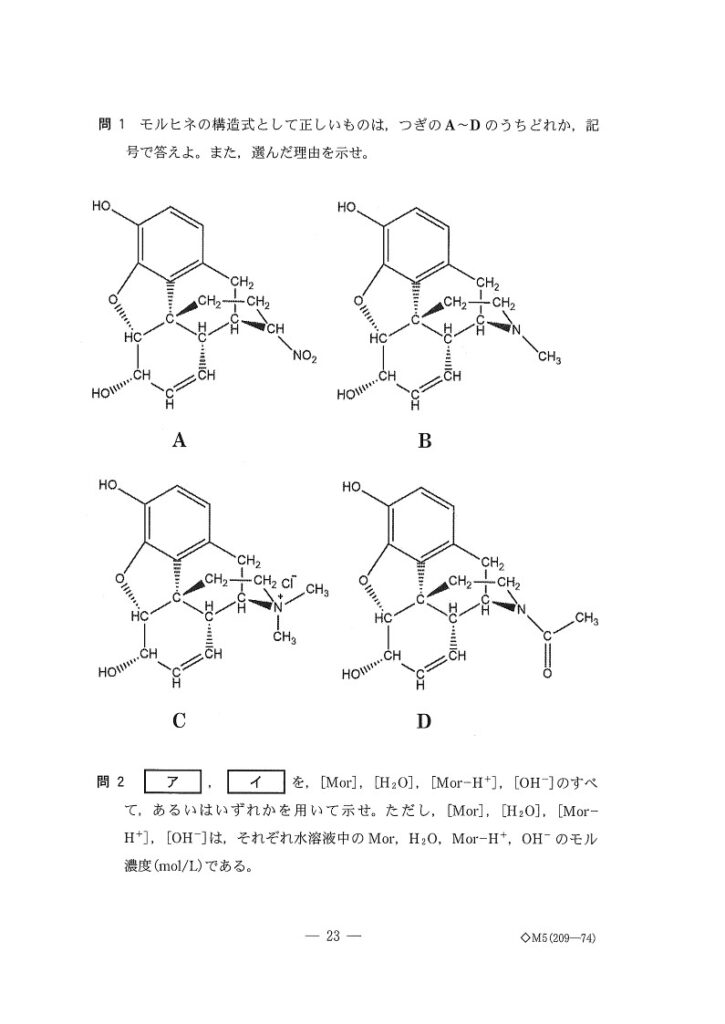
B
BのみがH⁺と結合できるから。
<分析>
モルヒネの構造式を知っている受験生は皆無でしょう。ここは、問題文中にヒントに考えます🤔
「N原子は非共有電子対をH+に与える」ので、N原子に着目し、非共有電子対をもつものを選択すればOK。
よって、BかDになるのですが、BとDの2択がえらく難しい🥲
Dを切る理由ですが…私は
「もしDのN原子にHが結合したとすると、アミド結合ができて、加水分解を受けるから。」と解釈しました。
(問2) 易
<分析>
これは電離定数の定め方を知っていれば楽勝です👋
(問3) 標準
(ⅰ),(ⅱ),(ⅳ)
<分析>
ルシャトリエの原理を理解したうえで、1つ1つ調査していけばできます。間違えるとすれば(ⅲ)でしょうか。
(ⅰ)
H⁺濃度が増えると、OH⁻濃度は減ります。ルシャトリエの原理より、①の平衡は右に移動しMor-H⁺濃度が増えます。(ⅱ)
(ⅰ)の逆で、OH⁻濃度が増えることでMor-H⁺濃度が減ります。
(ⅲ)
弱酸の電離度なんかを考えると、これは感覚的に×だとわかりますが…そもそも濃度を1/10にすると③の右辺の値は1/10になります。温度一定だと平衡定数も一定である点を考えると、(ⅲ)の記述は不適切です✋
(ⅳ)
Mor追加で①の平衡は右に移動しOH⁻濃度は増えるため、pHは大きくなります。(ⅴ)
(ⅳ)と逆の現象が起きるため×。
(問4) やや易
酸性
Mor-H⁺+ H₂O⇄Mor+H₃O+
<分析>
①の逆反応なんだから酸性でしょ?…という勘は働くでしょう。
現に、①の両辺にH⁺を加えると、左辺がH₃O⁺、右辺がH₂Oに化けるのは明らかでしょう。ここは、オキソニウムイオンを意識したい問題でした。
(問5) やや易〜標準
(1) 6.3×10⁻⁷(mol/L)
(2) 4.9×10⁻⁶(mol/L)
<分析>
(1)はpH=8よりOH⁻濃度が出ます。さらに[Mor- H⁺]=[OH⁻]に着目すると、[Mor]が出ます☝️
(2)は[Mor]+[Mor-H⁺]が電離前のモルヒネのモル濃度なので、これに×3.00することで総物質量が求められます。
(問6) やや易〜標準
<答>
<分析>
pH=7.4を[ H⁺]さらには[OH⁻]に変換し、電離定数の式を利用すると解けます。
<感想>
(問1)の2択(BとD)が一番むずかったですね🥲
(問4)〜(問6)は頻出の平衡計算の問題で、演習経験があれば全然難しくありません。
第3問
一応、問題の問題だけ。

第4問



【解答】
(問1) やや易
(1) 4.64(L)
(2)
(a) PbCl₂
(b) CuS
(c) Fe(OH)₃
(d) Na⁺
<分析>
スチレンの物質量がわかるので、(1)を利用するとスルホ基の物質量もわかります。あとは、体積をv(ml)として等式を解けば終わりです。
(2)については、熱水に溶ける塩化物、酸性条件下での硫化物、アンモニアとの錯イオン形成、炎色反応の基本的な知識があれば難しくありません。
(問2) やや易
1.2(mol/L)
<分析>
二クロム酸イオンと過酸化水素水の半反応式が書けるかどうかの問題。
書ければ、後は算数の問題です。
(問3) やや易
陽極:2Cl⁻→ Cl₂+2e⁻
陰極:2H₂O+2e⁻→ H₂+2OH⁻
全体:2H₂O+2Cl⁻ → H₂+Cl₂+2OH⁻
<分析>
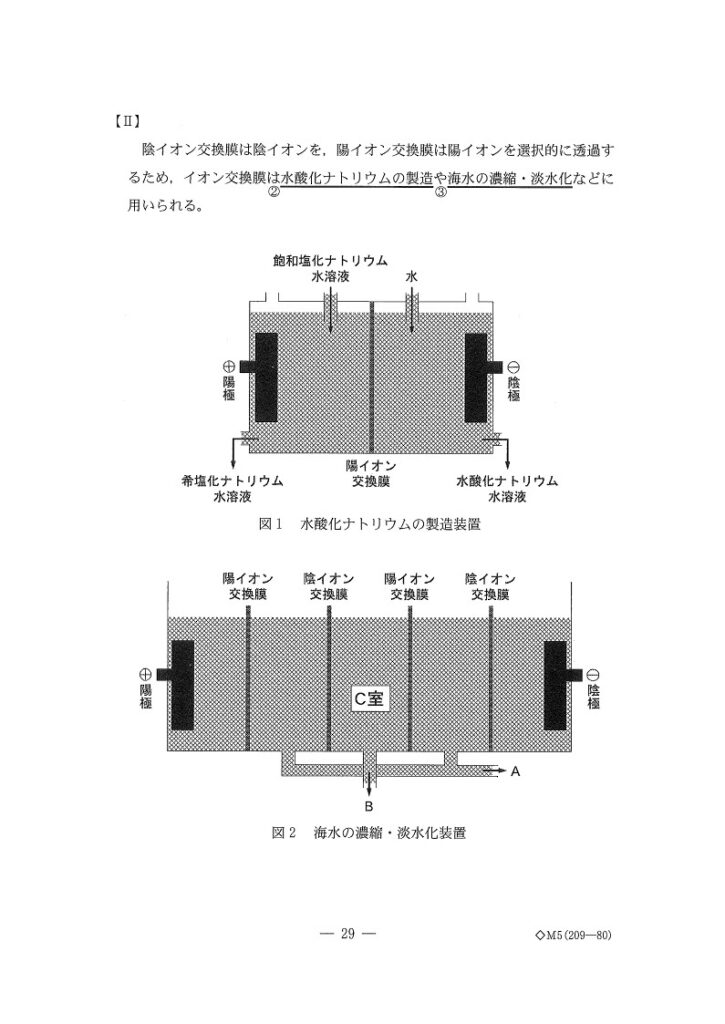
電気分解とイオン交換膜を経て高純度のNaOH溶液を生成するよくある問題です。
(問4) やや難
陽イオン交換膜がない場合、NaOHが陽極で発生したCl₂と2NaOH+ Cl₂ → NaCl+ NaClO+H₂Oの反応を起こして消費されるため。
<分析>
「反応式を用いて説明せよ」がヒントです💡
イオン交換膜がないと、陰極で生じたOH⁻は陽極の方まで到達してCl₂と反応します。
「Na+が陽イオン交換膜を経て陰極側に移動するため」なる解答も推測されますが、それでは反応式を用いた説明ができないため、今回は意図されていない答だと思いたかったですね😵💫
(問5) 標準
A>B
Na⁺は陽極から陰極側へ、Cl⁻は陰極から陽極側へ移動するから。
<分析>
陰極と陽極の反応より、溶液の電気的中性を保つように陽(陰)イオンがどう動くかを捉えましょう👀
(問6) 標準
(ア) イオン交換樹脂
(イ) 電気分解
(ウ) 交換
(エ) イオン交換膜
(オ) 濃縮
(カ) 再生
<分析>
水の電気分解で生じるのはOH⁻ですが、C室にイオン交換樹脂を充填したことで何が起きたかをきちんと把握したいところです🤔
OH⁻は陽イオン交換膜は通過できませんが、充填した陰イオン交換樹脂とは接することができるので、OH⁻とCl⁻の交換は可能となります☝️
<感想>
(Ⅰ)は陽イオン交換樹脂を題材にした理論化学の問題でした。高分子化合物は全く関係ありません🤥
(Ⅱ)は陽イオン交換樹脂を用いて高純度のNaOH溶液を生成する電気分解の問題で、これも非常によく見るタイプ。
総括
基礎〜標準レベルの問題が非常に多く、これは特に難しいと思う大問はなかったです👋
少し前の阪大化学からすると随分高得点が取りやすいセットになったな〜
と思わざるをえません😅
第3問は物議を醸した問題で省略したので、残りの第1,2,4問だけで考えると
合格点は
非医:65%
医:80%
程度でしょうか。
やはり、例年より高めの得点を取る必要はありそうです💦
最後に、再度公式LINEの紹介をします。
公立中出身から東大理Ⅲ,京大医学部のA判定に辿り着いた私が、大手予備校や受験秀才が言わない情報を存分に発信する公式LINEはこちら👇
登録していただいた方には、無料プレゼント贈呈🎁の他、無料相談も受け付けております。






