
受験生の皆さん、こんにちは。
東大合格ビジネスマンのワタシですm(_ _)m
私のブログでは
① 入試問題の解答・解説
② 受験合格に必要なマインド
③ 3大基礎力重視の裏ワザ勉強法
について、様々な観点から発信しております。
また、私の公式ラインでは無料相談を随時受け付けております。
公立中学出身から東大理Ⅲ,京大医学部のA判定に辿り着いた私が、大手予備校や受験秀才が言わない情報を存分に発信します。
成績が低迷しているのに1人で悩むのは時間の無駄ですから、いち受験のプロの私に相談してみてください✊
私も、できない科目は先生を頼りました。
また、LINE登録していただいた方には
無料プレゼント(1年で偏差値70出す画期的勉強法)
を贈呈します🎁
【⬇️公式LINE登録はこちら⬇️】

今回は
2022年の慶應理工の化学について解説します。
慶應理工の化学は、一部と私立大に見られる癖が強い問題はほぼありませんが、計算が結構厄介な傾向にあります。
さて、今年の化学はどうだったのか?
早速見ていきましょう👀
第1問

【解答】
(1)
(ア) ハーバー・ボッシュ
(イ)(NH₂)₂CO
(ウ) Al(OH)₃
<分析>
(ア) 易
暗記問題。硫酸の接触法や硝酸のオストワルト法と混同しないように注意しましょう!
(イ) やや易
時々顔を出す尿素・・・演習慣れしていれば解けたと思いますが、尿素を知らないと詰んだかも。合成の反応式は2NH₃+CO₂ → (NH₂)₂CO+H₂O。尿素の構造式はあまり出ませんが、難関大志望者なら覚えておきたいです。
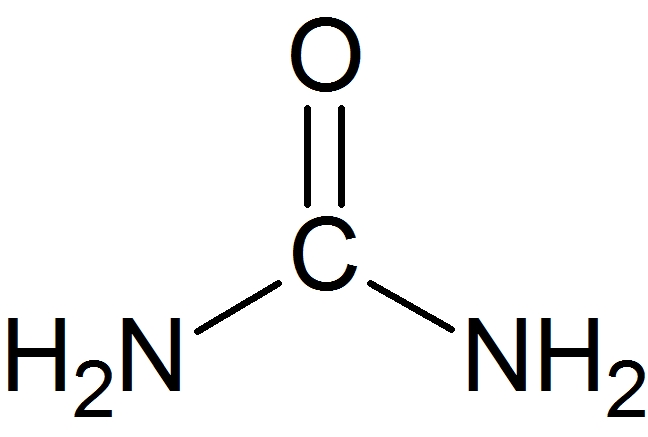
(ウ) やや易
アンモニアは弱塩基性。まず「水酸化物で沈殿を作らないのはどれか?」に着目すると、K⁺,Ca²⁺でしょう。残りのAl³⁺とZn²⁺については、「アンモニア分子と錯イオンを形成するのがどちらか?」で判断可能でしょう。
(2)
(エ) 4.0×10⁻⁵
(オ) 2.0×10⁻⁵(mol/L)
<分析>
(エ) やや易
加水分解定数Khを自分で設定して解く問題です。Kbだけを使って解くと間違えるので要注意!まあ、演習経験がマトモにあればできるレベルですが💦

(オ) やや易
(エ)の時点でhは相当小さい(10⁻⁵レベル)ので、濃度を4倍にしたところで依然1-h≒1が成り立つのだろうと推測は立つでしょう。実際に近似計算すると、h=2.0×10⁻⁵であることから裏付けはとれます。

(3)
(カ) 4
(キ) 3
(ク) 1.2(mol)
<分析>
(カ) 易~やや易
よく見る半反応式は O₂+4H⁺+4e⁻ → 2H₂Oですが、塩基性水溶液ではH₂OとOH⁻のみで表すのがお約束なので、本問ではO₂+2H₂+4e⁻→4OH⁻です。いずれにせよ、半反応式より、O₂1molあたりe⁻は4mol必要なことは明らか。
(キ) やや易
生成物はわかっているので、NH₃+ ? → N₂+ H₂O+?e⁻の形は作れますね。左辺の?はH₂Oで帳尻合わせすれば出ます。e⁻の係数を求めるのは、H₂O帳尻合わせでも出ますが、Nの酸化数変化(−3 → 0)に着目しても出ます☝
(ク) やや易
以下の計算で出ます。

(4)
(ケ) 0.36(Pa/min)
(コ) 2.4(Pa)
(サ) 表面積
<分析>
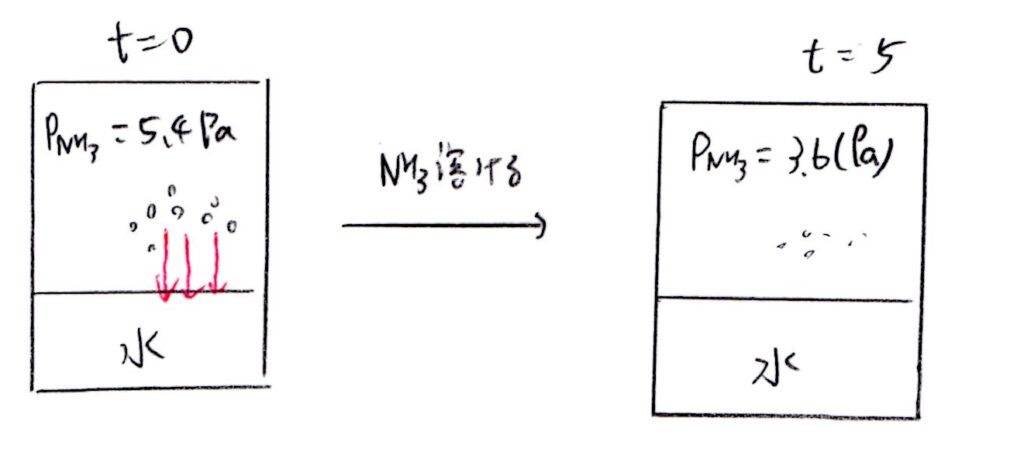
(ケ) 易
小学生レベルの算数です。5.4-3.6/5 =0.36(Pa/min)。
(コ) やや易
問題文の表現がわかりにくいですが、演習慣れしていれば「一次反応」のことを言っているんだなと理解できるでしょう💡t=0からの5分間でアンモニア分圧は2/3となりました。よって、t=10のときの分圧はt=5のときの2/3であると考えられます。
(サ) やや易~標準
体積と誤答しないように注意!!「同量の水」の記述より、水の総質量と総体積は変化ないと読み取れるため、体積だと×です。「表面積が大きいほど水の吸収が速い」って中学理科で聞いた話だなぁ・・・はい!
小腸の柔毛と同じ原理なのです😲🚩
以下では養分の吸収が力説されていますが、水の場合も同様です。

第2問

【解答】
(1)
(ア) 5.1(K・kg/mol)
(イ) 6.1×10⁻²(mol/kg)
(ウ) 78%
<分析>
(ア) 易
ベンゼンを溶媒、トルエンを溶質として考えます。なお、凝固点降下や沸点上昇で使う濃度はモル濃度とは違います。質量モル濃度ですよ✋

(イ) 易
(ア)の結果を使う問題ですが、解法は(ア)と同じ。

(ウ) やや易
安息香酸の二量体は有名ですね。ただ、本問では図示がされていないので、「二量体って何?」となって全くイメージができなかった受験生は解けなかったでしょう💦

(二量体のイメージ)
OとH間で水素結合してます!「なんで二量体を形成するのか?」という説明問題でも出てきそうですね🤔
(2)
(エ) 2.2×10⁻²(mol)
(オ) 1.0×10⁵(Pa)
<分析>
(エ) 易
浸透圧の公式(ファントホッフの式)を覚えていれば、何でもない問題です。
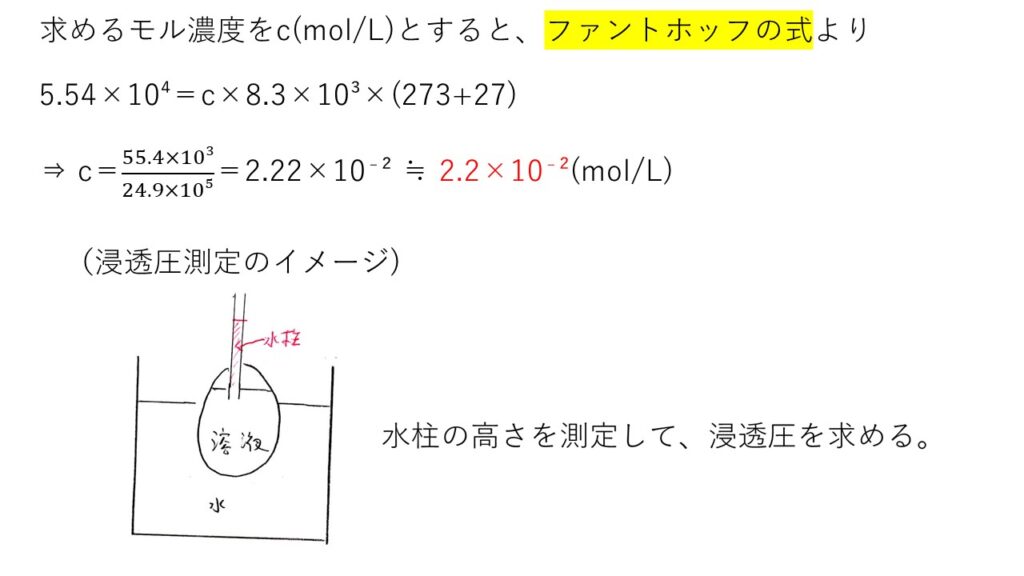
(オ) やや易
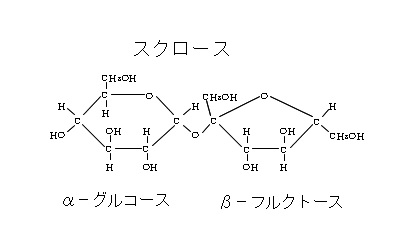
スクロース(二糖類)を知らん慶応受験生はヤバイです。なお、スクラーゼを加えると加水分解されてグルコースとフルクトース(分子式は同じC₆H₁₂O₆)を生成しますので、あとは解答のように処理すればOK!

(スクロースの構造式)
(3)
(カ) 2.7×10³(kJ)
(キ) 3.5×10³(kJ)
(ク) 8.9×10²(kJ)
<分析>
(カ) ,(キ) 易~やや易
超頻出問題なので、マトモな慶応受験生ならでできなきゃヤバイです。各分子の構造式が書けさえすりゃ楽勝です✋
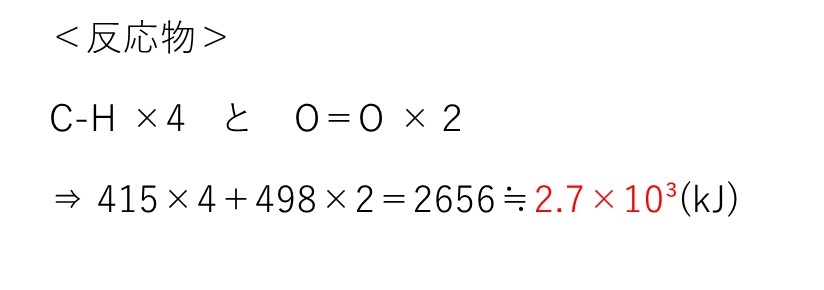

(ク) 標準~やや難
あ~!これは引っ掛け問題ですね💦
求めるのはQではないし、(カ)と(キ)の結果だけを使うと間違えます。
25℃なんだからH₂O(液)と気付きたいし、わざわざ(式2)の反応式が登場していることからもH₂O(液)が絡むのかな?と思いたいところでしたね😓まあ、メタンの燃焼熱891kJ/molはガチ勢には有名な数値なので、802kJ/molに違和感を覚えて修正できたかもしれませんが💦

(4)
(ケ) 1.0×10³(mol)
(コ) 4.0×10⁻³(mol)
(サ) 2.4×10⁴(Pa)
<分析>
(ケ) 易~やや易
プロパンの分圧:2.75×10⁴−2.50×10⁴=0.25×10⁴(Pa)を出して状態方程式を使う問題です。

(コ) やや易
炭化水素を燃焼するとCO₂とH₂Oを生じるのは受験化学の常識として覚えるべし。O₂の係数についてはCO₂とH₂Oの係数を確定してから帳尻合わせでOK。
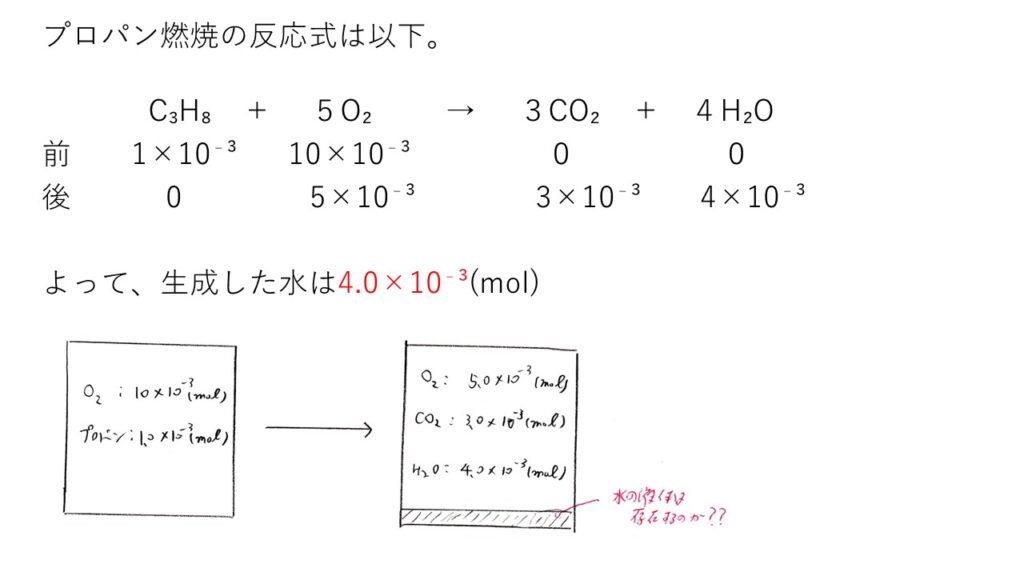
(サ) やや易~標準
液体が存在するのかどうかわからん場合に「もし全部気体だとすると」と仮定する解法は王道パターンです。

第3問

【解答】
まず情報整理!

(1)
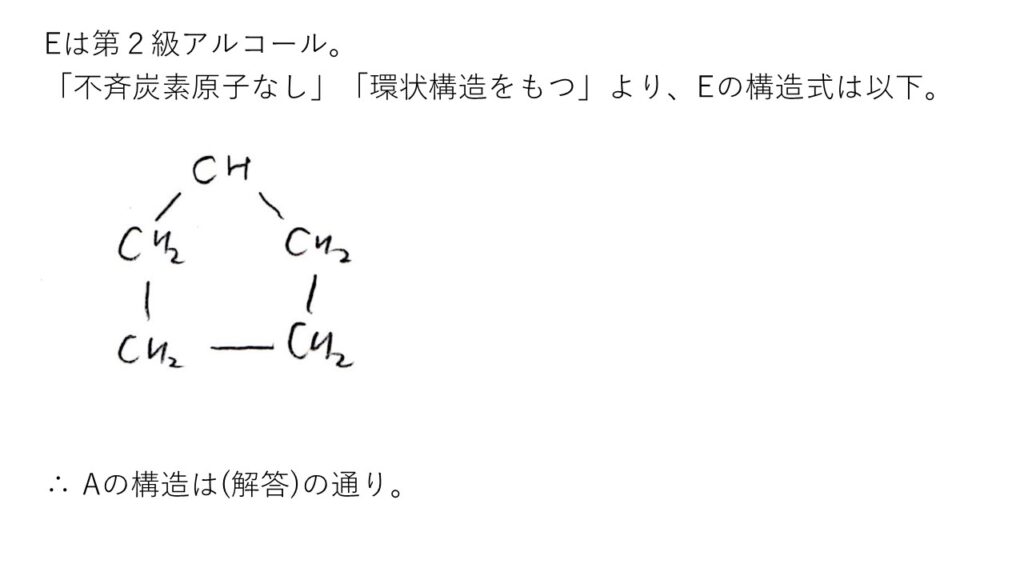
(ⅰ) やや易
(ア) テレフタル酸
(イ) C₅H₁₂O
(ウ)

<分析>
(ア)~(ウ)


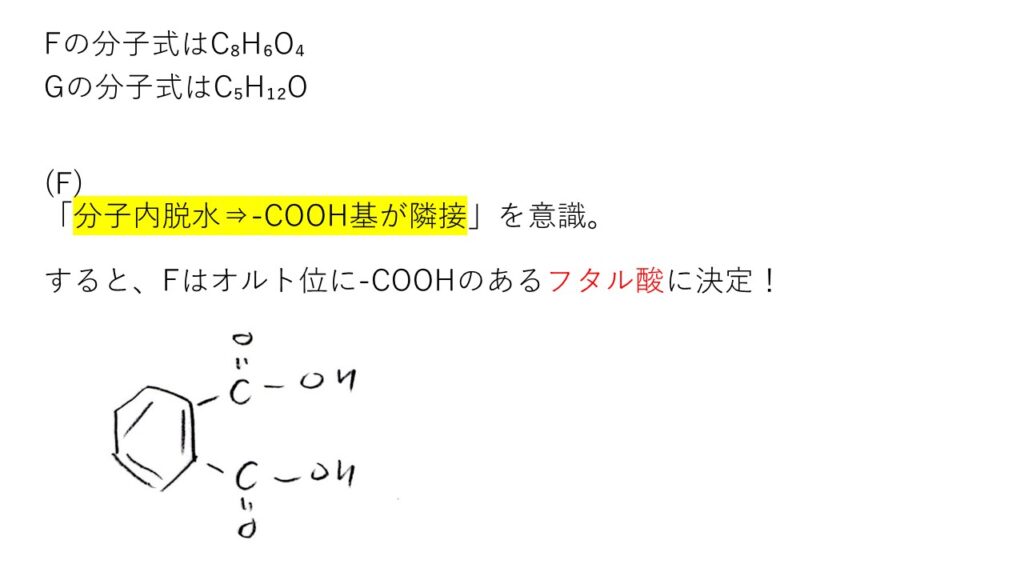
(ⅱ) やや易
(エ) フタル酸
(オ)

(カ)

<分析>

(ⅲ) やや易~標準
(キ) サリチル酸
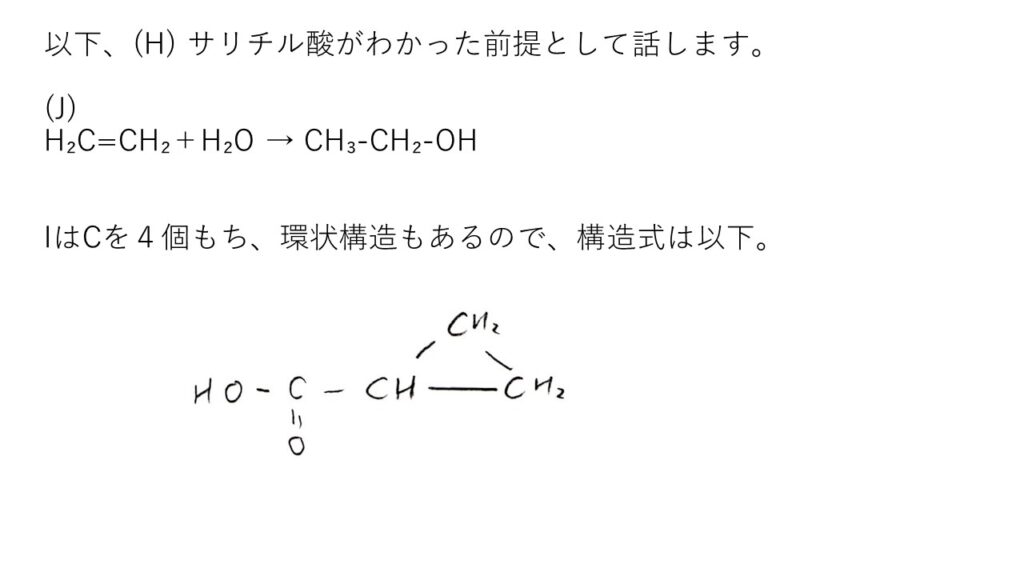
(ク)

<分析>
以下の反応は暗記しておきましょう👇

(2) やや易
(ケ) 1134
(コ)

<分析>
(ケ)
実際に簡略化して書いてみると、水分子が計7個とれることになります。よって、分子量は180×7−18×7=1134。

(コ)
グルコースの構造式は暗記必須!1,4位の-OHが結合に使われているので、-OHが-OCH₃になるのは2,3,6位の-OHです。
(3) やや易
(サ)
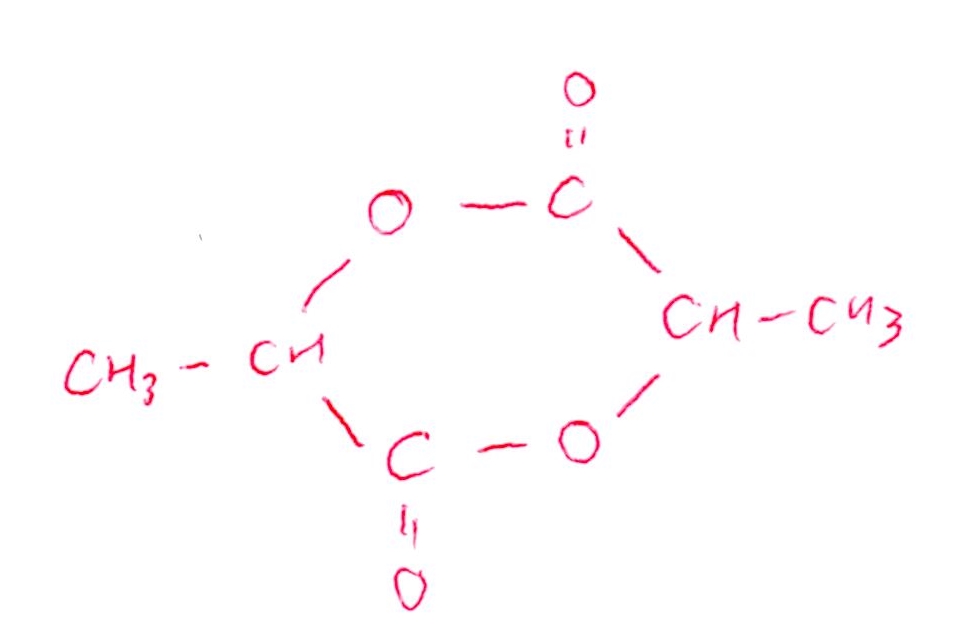
(シ) 生分解性
<分析>
(3)は知識問題と言ってもいいでしょう。「乳酸(C₃H₆O₃)の構造式を知ってますか?」だけの問題です。
語句「生分解性」は2021年の九大化学にも登場しました👋
総括
以上で、慶應理工の化学の解説を終わります。
私的な感想では、基礎的理解と盤石な計算力があれば9割得点は全然いけるレベルでした。
東大理系志望なら、8割切っちゃまずいレベルですね💦
最後に、再度公式ラインの紹介をします。
私の公式LINEでは、無料相談を随時受け付けております。
成績が低迷しているのに1人で悩むのは時間の無駄ですから、受験のプロを頼ってみてください✊
【⬇️公式LINE登録はこちら⬇️】





